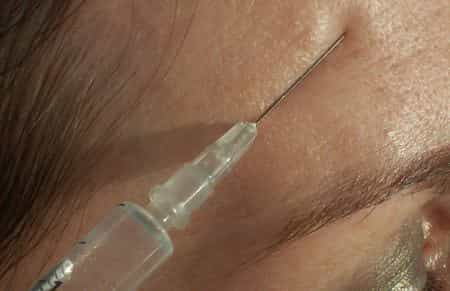
Botox es el nombre comercial más conocido del preparado farmacológico que utiliza como ingrediente activo la toxina botulínica, una proteína neurotóxica producida por la bacteria Clostridium botulinum, para el lifting facial. La toxina botulínica es un polipéptido de doble cadena, con una cadena de 100 kDa unida mediante enlaces disulfuro a otra cadena de 50 kDa. La cadena ligera es una enzima proteasa que ataca a una de las proteínas (SNAP-25, sintaxina o sinaptobrevina) de la unión neuromuscular, impidiendo la liberación de acetilcolina de las vesículas. Al inhibir la liberación de este neurotransmisor, la toxina interfiere con el impulso nervioso y provoca una parálisis fláccida de los músculos característica del botulismo y en contraste con la parálisis espástica observada en el tétanos. Estos últimos días, gracias a un artículo del periódico londinense The Sun, ha salido a la luz la otra cara de la moneda: los peligros de las inyecciones de Botox, que en algunos casos pueden incluso provocar la muerte. Sólo el año pasado en Inglaterra hubo al menos dieciséis víctimas, entre ellas cuatro menores. Los médicos plantean la hipótesis de que la causa de la muerte es el hecho de que la toxina botulínica introducida en el organismo puede expandirse hacia los tejidos cercanos, como el esófago, paralizando o, en cualquier caso, limitando gravemente las funciones del órgano. El porcentaje de pacientes fallecidos como consecuencia de las 55.000 inyecciones no es elevado (menos de una persona entre mil), pero como piden algunas asociaciones de consumidores es necesario -con razón- incluir en las contraindicaciones todos los efectos adversos que puede tener llegar a. En 1937 Alan B. Scott, oftalmólogo del Instituto Smith-Kettlewell, utilizó la toxina botulínica A (BTX-A) en experimentos con monos, y en 1980 utilizó la BTX-A por primera vez en humanos para tratar el estrabismo. La BTX-A fue aprobada en 1989 por la Administración de Alimentos y Medicamentos para el tratamiento del estrabismo, blefaroespasmo y espasmo hemifacial en pacientes mayores de 12 años. En 2002 se aprobó su uso en medicina estética para la mejora temporal de las líneas de expresión entre las cejas (líneas glabelares) mediante pequeñas inyecciones en la piel que tienen un efecto de relajación muscular durante hasta 4-5 meses. [más información ]
También te puede interesar
Reducir el colesterol con leche fermentada
Las leches fermentadas adicionadas con fitoesteroles son capaces de reducir el nivel de colesterol malo en aproximadamente un 10% en sujetos con hipercolesterolemia moderada. Así lo demuestra el primer metaanálisis realizado con aproximadamente 400 personas que analizó los resultados de 3 trabajos ya publicados en la literatura sobre el efecto de una leche fermentada con… Continua a leggere Reducir el colesterol con leche fermentada
Dieta probiótica
Con la llegada de la temporada de frío aumentan las infecciones bacterianas y por tanto el uso de antibióticos, que pueden alterar el equilibrio intestinal normal. Los niños y los ancianos corren un riesgo especial. Por lo tanto, es mejor seguir una " dieta probiótica ", que incluya el consumo de probióticos que se utilizarán… Continua a leggere Dieta probiótica
Bótox para la nariz
En un artículo de la semana pasada hablábamos de la toxina botulínica para uso puramente clínico, en patologías neuromusculares, para las que se acaban de definir las pautas de tratamiento. El Botox se utiliza ahora de forma amplia y sencilla, especialmente en cirugía estética y no sólo para las arrugas sino también para corregir la… Continua a leggere Bótox para la nariz